Chưa có sản phẩm trong giỏ hàng.
Lịch sử phát hiện và sử dụng amoniac
Người Roman xưa đã tìm thấy muối amoni clorua tại đền thờ thần Jupiter tại xứ Libi cổ và gọi muối đó là “ muối Amun” ( salt of Amun). Trong một tác phẩm cổ, Caius Plinius Secundus (hay còn gọi là Pliny the Elder) có nhắc đến tên một loại muối được gọi là “Hammoniacus” (hammoniacus sal, hay còn gọi là sal ammoniac). Vào Thế kỷ thứ 8, các nhà giả kim thuật Arập đã biết đến sal ammoniac. Sau đó vào Thế kỷ 13, Geber (Jabir ibn Hayyan) và các nhà giả kim thuật châu Âu cũng nhắc đến tên muối này. Vào thời kỳ Trung thế kỷ, những người thợ nhuộm đã biết dùng muối sal ammoniac (còn được gọi là nước tiểu lên men) để làm đổi màu các loại thuốc nhuộm có nguồn gốc thảo mộc. Vào Thế kỷ 15, Basilius Valentinus đã chỉ ra rằng có thể thu được amoniac bằng các cho kiềm tác dụng với sal ammoniac. Sau đó loại muối này đã được điều chế bằng cách chưng (nhiệt phân) sừng và móng gia súc, sau đó trung hòa dịch cất chứa cacbonat thu được với axit clohyđric (HCl).
Lần đầu tiên amoniac dạng khí do Joseph Priestley phân lập vào năm 1774 và được ông đặt tên là “không khí kiềm” (alkaline air). Tuy nhiên người đầu tiên thu được chất khí này là nhà giả kim thuật Basil Valentine. 11 năm sau, Claude Louis Berthollet đã xác định được thành phần phân tử của amoniac là NH3.
Fritz Haber và Carl Bosch là những người phát hiện quy trình sản xuất amoniac vào năm 1909. Công trình này đã được đăng ký phát minh vào năm 1910.
Người Đức là là những người đầu tiên trên thế giới sử dụng amoniac ở quy mô công nghiệp trong thời kỳ Đại chiến thế giới lần thứ I sau khi bị phong tỏa mất nguồn natri nitrat từ Chilê. Khi đó amoniac được được người Đức dùng để sản xuất thuốc nổ phục vụ chiến tranh.
Các nguồn phát sinh amoniac
Hiện nay ngoài nguồn NH3 nhân tạo (các nhà máy sản xuất phân urê hoặc các nhà máy chuyên sản xuất amoniac lỏng), trong tự nhiên cũng có một lượng nhỏ NH3 tồn tại trong khí quyển do thường xuyên hợp chất này được tạo ra từ các quá trình phân hủy các vật liệu hữu cơ có nguồn gốc động, thực vật.
Trong nước mưa, nước biển người ta cũng phát hiện thấy có NH3 và các các muối amoni. Hoạt động của núi lửa cũng là nguồn sinh ra muối amoni (như amoni clorua NH4Cl và amoni sunfat (NH4)2SO4). Tại một số vùng khoáng chứa sôđa, người ta cũng thấy có các tinh thể amoni bicacbonat NH4HCO3. Các hoạt động sinh hóa hàng ngày của người và động vật cũng là nguồn sinh ra NH3.
Một số tính chất cơ bản của amoniac
1. Tính chất vật lý
Amoniac có công thức phân tử là NH3. Phân tử lượng NH3 là 17,0306g/mol.
Ở điều kiện thường, NH3 khan là một chất khí không màu, nhẹ bằng nửa không khí (tỷ trọng so với không khí bằng 0,596 ở OoC), có mùi sốc đặc trưng.
Amoniac khan tạo “khói” trong không khí ẩm. Amoniac hòa tan mạnh trong nước tạo thành dung dịch nước của NH3 (hay còn gọi là amoni hyđroxit do trong dung dịch nước của amoniac có tạo thành NH4OH). Ở OoC, NH3 có độ hòa tan cực đại là 89,9g trong 100 ml nước. Dung dịch nước của NH3 (còn có tên là “ nước đái quỷ”) khá bền nhưng bị loại gần hết NH3 khi đun tới sôi.
Nồng độ của amoni hyđroxit có thể được xác định bằng tỷ trọng kế hoặc Bomé kế.
Ở áp suất khí quyển, NH3 hóa lỏng tại -33,34oC (239,81oK), có trọng lượng riêng 682 g/lit tại 4oC, hóa rắn tại -77,73oC (195,92oK), vì vậy ở nhiệt độ thường người ta phải lưu trữ NH3 lỏng dưới áp suất cao (khoảng trên 10 atm tại 25,7oC).
Do NH3 lỏng có entalpy (nhiệt bay hơi) ∆H thay đổi lớn (23,35kJ/mol) nên chất này được dùng làm môi chất làm lạnh.
NH3 lỏng là một dung môi hòa tan tốt nhiều chất và là một trong những dung môi ion hóa không nước quan trong nhất. Nó có thể hòa tan các kim loại kiềm, kiềm thổ và một số kim loại đất hiếm để tạo ra các dung dịch kim loại (có màu), dẫn điện và có chứa các electron solvat hóa.
Một số tính chất đặc trưng của NH3
| Điểm sôi (ở áp suất khí quyển) | -33,34°C |
| Tỷ trọng (so với không khí ở OoC) | 0,596 |
| Độ hòa tan trong nước g/100g H2O | 89,9 (OoC) 60 (ở 15°C) 7,4 (100°C) |
| Độ tan của NH3 khí trong 1 lit nước | 700 lít (20°C) |
| Giới hạn nổ với không khí | 15-28% (thể tích) |
NH3 lỏng là một dung môi ion hóa nhưng yếu hơn nước. Nó có thể hòa tan và phân li nhiều hợp chất có liên kết ion điển hình như các muối nitrat, nitrit, xyanua, v.v …của kim loại kiềm và amoni. Trong NH3 lỏng, các muối amoni tan đều có tính axit. So với trong môi trường nước, thế oxyhóa khử của nhiều hệ trong NH3 lỏng đều chuyển sang dương hơn.
2. Tính chất hóa học
Phân tử NH3 có cấu trúc kim tự tháp tam giác (trigonal pyramid).
Trong không khí, NH3 là chất bền, không tự bốc cháy và không duy trì sự cháy. Ở nhiệt độ cao (1200oC) và có mặt của chất xúc tác thích hợp, amoniac có thể bị phân hủy thành nitơ và hyđro.
2NH3 → N2 + 3H2 t°= 1200°C (1)
NH3 có thể phản ứng với các chất oxy hóa. Ví dụ: nó có thể cháy trong oxy với ngọn lửa màu lục vàng yếu cho sản phẩm là nitơ và nước; có thể cháy trong khí clo, nitơ bị đẩy ra và tạo HCl, còn trong trường hợp dư NH3 thì có thể xảy ra nổ mạnh đồng thời tạo thành nitơ triclorua NCl3. Khi đó nitơ trong phân tử NH3 chuyển hóa trị từ – 3 lên +3.
Cũng vì lẽ NH3 dễ dàng phản ứng với nhiều chất, trong đó có các chất oxy hóa mạnh, các axit mạnh, v.v…, nên trong thực tế người ta khuyến cáo không nên trộn lẫn (hoặc để gần) amoniac với các axit mạnh, các halogen, các chất chất tẩy trắng clorin (chlorine bleach) hoặc các chất oxy hóa mạnh khác.
NH3 khan (độ ẩm dưới 0,2%) không phản ứng với HCl khan, tuy nhiên khi có mặt của nước (độ ẩm) sẽ xảy ra phản ứng mạnh. Trong trường hợp này, NH3 thể hiện tính bazơ điển hình. Dung dịch nước của amoniac thường được gọi là amoni hyđroxit với hằng số bazơ pk=4,75, và tác dụng tỷ lượng với các axit và tạo các muối amoni. Ví dụ:
NH3 + HCl → NH4Cl (2)
Phản ứng tạo khói trắng rất đặc trưng khi cho hơi NH3 tiếp xúc với dung dịch HCl đậm đặc.
Trong khi đó bản thân NH3 khan lại là một axit rất yếu, có thể mất 1 proton H+ tạo thành anion amid NH2–. Ví dụ cho liti nitrua vào NH3 lỏng người ta nhận được anion amid (NH2– )
Li3N(s)+ 2 NH3 (l) → 3 Li+(am) + 3 NH2−(am) (3)
Hyđro trong NH3 có thể bị các kim loại mạnh đẩy ra và thế chỗ để tạo ra các nitrua như magie có thể cháy trong NH3 để tạo magie nitrua Mg3N2. Natri hoặc kali kim loại nóng có thể tạo ra các nitrua (NaNH2, KNH2) khi tác dụng với NH3.
NH3 có thể bị oxy hóa thành axit nitric HNO3 với sự có mặt của xúc tác platin ở nhiệt độ 750-800oC, áp suất oxy 9 atm. Quá trình này được gọi là quá trình Oswald
4 NH3 + 8 O2 → 4 HNO3 + 4 H2O (4)
Từ axit nitric người ta có thể sản xuất nhiều dẫn xuất của nitơ trong đó có các chất nổ.
NH3 tự bốc cháy ở 651 °C và có thể tạo hỗn hợp nổ với không khí khi nồng độ nằm trong vùng 16–25% (có tài liệu nói là 16-28%).
NH3 có tính ăn mòn các kim loại và hợp kim chứa đồng (Cu), kẽm (Zn), nhôm (Al), vàng (Au), bạc (Ag), thủy ngân (Hg), v.v… Vì vây trong thực tế người ta khuyến cáo không nên để hơi hoặc dung dịch amoniac tiếp xúc với các vật dụng có chứa các kim loại hoặc hợp kim này. Khi NH3 tiếp xúc lâu dài với một số kim loại (Au, Ag, Hg, Ge, Te, Sb…) thì có thể tạo ra các hợp chất kiểu fuminat dễ gây nổ nguy hiểm.
Amoniac lỏng phá hủy các chất dẻo, cao su, gây phản ứng trùng hợp nổ của etylen oxit.
Công nghệ sản xuất amoniac
Trước Đại chiến Thế giới lần I, NH3 được điều chế ở quy mô rất nhỏ bằng cách chưng cất các chất thải động thực vật, than đá, hoặc cho các muối amoni, nhất là amoni clorua (sal ammoniac), tác dụng với kiềm (vôi). Phản ứng xảy ra như sau:
2 NH4Cl + 2 CaO → CaCl2 + Ca(OH)2 + 2 NH3 (5)
Mặc dù trong không khí rất sẵn nitơ, nhưng phải đến đầu Thế kỷ 20, nhờ phản ứng cố định nitơ con người mới có thể sản xuất NH3 và các hợp chất chứa đạm khác ở quy mô công nghiệp.
Hai nhà hóa học người Đức (Fritz Haber và Carl Bosch) là những người đầu tiên phát hiện quy trình sản xuất amoniac vào năm 1909 và công trình này đã được đăng ký phát minh vào năm 1910.
Quy trình Haber (hay còn gọi là quy trình Haber-Bosch) là quy trình dựa trên phản ứng cố định nitơ bằng hyđro trên nền sắt (xúc tác) để tạo ra NH3 . Đây là một phản ứng vô cùng quan trọng vì nó là cơ sở để sản xuất NH3 ở quy mô công nghiệp phục vụ sản xuất phân đạm.
Các công nghệ sản xuất NH3 mang tên khác nhau được đăng ký phát minh về sau này chủ yếu vẫn dựa trên nguyên tắc cố định nitơ bằng hyđro của Haber-Bosch trên cơ sở thay đổi nguyên liệu đầu, chất xúc tác và các điều kiện phản ứng (áp suất, nhiệt độ, v.v…).
Hiện nay trên thế giới có một số công nghệ sản xuất amoniac đang được áp dụng thương mại, trong đó có 5 công nghệ được thương mại hóa nhiều nhất là:
1/ Công nghệ Haldor Topsoe ;
2/ Công nghệ M.W. Kellogg;
3/ Công nghệ Krupp Uhde;
4/ Công nghệ ICI;
5/ Công nghệ Brown & Root.
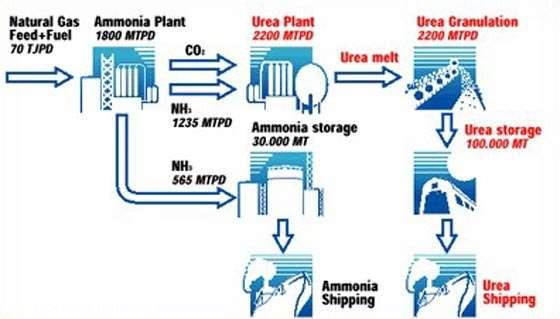
Riêng công nghệ Haldor Topsoe hiện chiếm đến 50% thị phần trên thị trường công nghệ trong lĩnh vực tổng hợp amoniac trên thế giới. Hiện các nhà máy sản xuất amoniac (và phân đạm) hiện đại nhất trên thế giới đều chuyển nguyên liệu đầu, ví dụ khí thiên nhiên (chủ yếu là metan NH4), khí hóa lỏng (chứa propan và butan), hoặc naphta, than đá thành khí tổng hợp (syngas) có chứa hyđro (H2) và cacbon monooxit (CO). Tiếp theo H2 được tách từ syngas (sau khi chuyển CO thành CO2 và được loại đi). Nitơ (N2) được lấy từ không khí sau khi tách hết oxy trong quá trình khí hóa nguyên liệu chứa cacbon.
Sau các quá trình rửa khí và điều chỉnh tỷ lệ N2:H2 người ta tiến hành tổng hợp NH3 bằng quá trình Haber–Bosch theo phản ứng:
3 H2 + N2 → 2 NH3 (6)
Trong một số trường hợp, người ta có thể lấy hyđro từ các nguồn khác (ví dụ điện phân).
Tại Việt Nam, các nhà máy phân đạm mới được xây dựng hoặc đang được xây dựng đều áp dụng quy trình công nghệ tổng hợp amoniac của hãng Haldor Topsoe như: Nhà máy Phân đạm Phú Mỹ của PetroVietnam tại Bà Rịa- Vũng Tầu (đi từ khí tự nhiên) ký mua bản quyền công nghệ năm 2002, Nhà máy Phân đam Ninh Bình của VINACHEM tại Ninh Bình (đi từ than đá) ký năm 2007, Nhà máy Phân đạm Cà Mau của PetroVietnam tại Cà Mau (đi từ khí thiên nhiên) ký năm 2008. Các nhà máy này hiện đã đưa vào sử dụng và cho ra sản phẩm.
Ứng dụng amoniac
Amoniac được sử dụng cả trong công nghiệp và trong đời sống hàng ngày. Cụ thể:
– Dung dịch nước của NH3 có nồng độ 25% hoặc thấp hơn thường được dùng trong các phòng thí nghiệm và trong đời sống.
– Dung dịch NH3 được sử dụng trong nông nghiệp như: tạo môi trường chống đông (nồng độ NH3 0,03% và axit boric 0,2-0,5%) để bảo quản mủ cao su (latex) hoặc được sử dụng trực tiếp làm phân bón.
– Dung dịch amoniac hoặc amoniac lỏng được sử dụng trong xử lý môi trường nhằm loại các NOx hoặc SOx trong các các khí thải khi đốt các nguyên liệu hóa thạch (than đá, dầu, v.v…). Quá trình này thường có thể phải dùng chất xúc tác chứa vanađi.
– Dung dịch amoniac hoặc amoniac lỏng được sử dụng trong công nghiệp sản xuất phân bón, hóa chất và hóa dược.
Tại Việt Nam hiện nay có 4 cơ sở có sản xuất NH3, đó là Công ty TNHH một thành viên Phân đạm và Hóa chất Hà Bắc, Công ty TNHH Đạm Ninh Bình (VINACHEM) công suất 560 nghìn tấn urê/năm và Nhà máy đạm Phú Mỹ (Bà Rịa- Vũng Tàu), Nhà máy đạm Cà Mau thuộc Tập đoàn Dầu khí Việt Nam (PetroVietnam). Hai nhà máy Đạm của VINACHEM sử dụng nguyên liệu chính từ than, còn 2 nhà máy Đạm của PetroVietnam sử dụng nguyên liệu đầu vào là khí thiên nhiên. Ngoài ra còn một dự án về sản xuất phân đạm cũng đang được chuẩn bị đầu tư như: Dự án sản xuất phân đạm từ than tại Nghi Sơn (Thanh Hóa) và một số dự án khác.
Công ty TNHH một thành viên Phân đạm và Hóa chất Hà Bắc chuyên sản xuất phân urê từ nguồn nguyên liệu than đá (dạng cục) do Trung Quốc giúp xây dựng từ năm 1960 nhưng do chiến tranh và nhiều khó khăn khác mà đến năm 1973 Nhà máy mới có sản phẩm urê. Nhà máy có công suất thiết kế ban đầu 10 nghìn tấn urê/ năm. Năm 1977 Nhà máy chính thức đi vào sản xuất sau khôi phục. Thời kỳ 2000-2003 Nhà máy được cải tạo kỹ thuật nâng công suất lên 150 nghìn tấn urê/năm và chạy ở công suất 180 nghìn tấn urê/năm từ đó đến nay. Bên cạnh sản xuất urê, Nhà máy cũng có khả năng cung cấp CO2 lỏng và rắn, năng lượng điện và 5-10 nghìn tấn NH3 lỏng/năm tùy theo nhu cầu thị trường.
Sản phẩm NH3 lỏng của Nhà máy đạt độ tinh khiết 99,9% và đã đạt được một số giải thưởng, huy chương (Huy chương Vàng Hội chợ Kinh tế Quốc dân năm 1986, 1988; Huy chương Vàng Hội chợ Kinh tế hàng công nghiệpViệt Nam năm 1993; Huy chương vàng Hội chợ Quốc tế Hóa chất Việt Nam năm 1997; Giải thưởng Bông lúa Vàng Hội chợ Nông nghiệp Quốc tế Cần Thơ năm 1997).
Nhà máy Phân đạm Phú Mỹ chuyên sản xuất urê từ nguồn khí thiên nhiên, khánh thành và bắt đầu đi vào sản xuất từ cuối năm 2004. Nhà máy có công suất thiết kế 760 nghìn tấn urê/năm. Ngoài sản phẩm urê, Nhà máy còn có năng lực cung cấp năng lượng điện và 90-100 nghìn tấn NH3/năm tùy theo nhu cầu thị trường.
Sản phẩm NH3 lỏng của Nhà máy đạt độ tinh khiết 99,9%; hàm lượng nước nhỏ hơn 0,1%; hàm lượng sắt nhỏ hơn 2mg/lít; hàm lượng đồng nhỏ hơn 8mg/lít.
Nguồn : hoahoacngaynay
